Содержание
Миелодиспластический синдром (МДС) – группа заболеваний костного мозга, для которых характерно снижение продукции одного или нескольких типов клеток крови (тромбоцитов, лейкоцитов, эритроцитов). Это приводит к анемии, рецидивирующим инфекциям и склонности к кожной геморрагии и кровоточивости слизистых оболочек. МДС может возникать спонтанно (de novo, без видимых причин, первичный МДС) или развиваться после применения определенных лекарств, химических веществ, радиации (вторичный МДС).
МДС – это когда костный мозг продуцирует недостаточное количество здоровых клеток крови
Нормальный костный мозг — это строма (скелет органа), образованная фиброзной тканью, а также собственно кроветворная ткань. Он в основном содержится внутри тазовых костей, в ребрах, грудине, костях черепа, длинных трубчатых, небольшое его количество находится в телах позвонков. По мере необходимости стволовые клетки костного мозга делятся, их клоны проходят стадии дифференцировки, осуществляется процесс создания новых клеток крови взамен погибающих и отмирающих. Процесс дифференцировки происходит по нескольким направлениям — стволовые клетки стремятся стать клетками определенного типа. В норме только полностью созревшие клетки попадают в кровоток. Они могут стать:
- Красными кровяными тельцами (эритроциты) — клетки, которые содержат гемоглобин и переносят кислород от лёгких к тканям.
- Белыми кровяными тельцами (лейкоциты) — пять различных видов клеток, которые борются с инфекциями.
- Маленькими кровяными пластинками (тромбоциты) — особый вид форменных элементов крови, которые при необходимости «закрывают» раны и останавливают кровотечение.
МДС иногда называют предлейкемией, гемопоэтической дисплазией, подострым миелоидным лейкозом, олигобластным лейкозом или тлеющим лейкозом
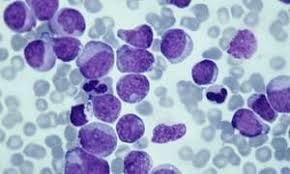
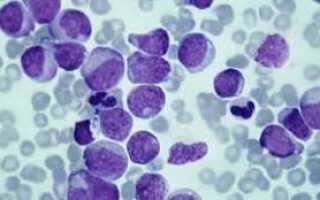
МДС начинается с повреждения или мутации ДНК в одной гемопоэтической (кроветворной) стволовой клетке. В результате чего в костном мозге начинает «перепроизводство» клеток крови. Он насыщается незрелыми или «бластными» клетками.
При МДС также наблюдается повышение запрограммированной гибели клеток (апоптоза), что приводит к интересному парадоксу. Хотя в костном мозге образуется больше клеток, чем в норме, но из-за того, что они живут недолго, в кровь их поступает меньше, чем необходимо. Поэтому люди с МДС часто страдают от анемии (низкий уровень эритроцитов), тромбоцитопении (низкий уровень тромбоцитов) и нейтропении (низкий уровень лейкоцитов в крови).
Люди с редкими наследственными синдромами подвержены повышенному риску заполучить МДС. К ним относятся синдром Швахмана-Даймонда, анемия Фанкони, врожденный дискератоз, синдром Даймонда-Блэкфана, наследуемые тромбоцитопатии и миелодисплазия. Перечислены нозологии объединяются под общим названием «синдромы наследственной недостаточности костного мозга».
МДС — это группа заболеваний, которые очень отличаются по течению и прогнозу. Некоторые из них «тлеют» на протяжении многих лет, они проявляются малозаметное симптоматикой и могут оставаться «недиагностированными» годами, пока дефицит клеток в кровотоке не отстанет значительным или болезнь не начнет быстро прогрессировать. Другие случаи МДС более агрессивны и быстро прогрессируют в самом начале болезни.
Типы
Миелодиспластический синдром классифицируется с использованием нескольких систем, разработанных группой международных экспертов. Эти классификации претерпевали изменения с течением времени. Они учитывают количество циркулирующих в кровотоке различных типов клеток, предполагаемую причину и прогностические критерии заболевания. Классификация МДС помогает прогнозировать течение болезни, определить оптимальную тактику лечения.
Врачи подчеркивают, что миелодиспластический синдром (МДС) требует комплексного подхода к диагностике и лечению. Основные анализы, которые назначаются пациентам, включают общий анализ крови, биохимию и морфологическое исследование костного мозга. Эти исследования помогают определить степень нарушения кроветворения и выявить аномалии в клетках. Прогностические критерии, такие как наличие цитогенетических изменений и уровень бластов в костном мозге, играют ключевую роль в оценке тяжести заболевания и выборе терапии. Лечение МДС может варьироваться от поддерживающей терапии до более агрессивных методов, таких как химиотерапия или трансплантация стволовых клеток. Врачи акцентируют внимание на индивидуальном подходе к каждому пациенту, учитывая его возраст, общее состояние и сопутствующие заболевания.

Классификация Всемирной организации здравоохранения (ВОЗ)
На сегодняшний день общепринятой считается классификация ВОЗ 2016 года, которая учитывает изменения клеточного состава в крови и костном мозге, а также наличие тех или иных хромосомных изменений (цитогенетика). В таблице приведены различные типы миелодиспластического синдрома:
| Вариант | Изменение в крови и костном мозге | Бласты | Комментарии |
| МДС с однолинейной дисплазией (MDS-SLD) | уменьшение количества одного или двух типов клеточных элементов крови*; дисплазия только одного ростка в костном мозге | Нет или меньше 1 % в крови; в костном мозге <5% | Прогноз хороший, как правило, люди с этим типом живут долго |
| МДС с кольцевыми сидеробластами (MDS-RS) | ≥ 15 % незрелых эритроцитов в костном мозге имеют кольцевидные скопления железа вокруг ядра (кольцевые сидеробласты). Если только один тип клеток костного мозга выглядит ненормальным, то это MDS-RS-SLD, а если два или все три типа — MDS-RS-MLD. | Нет или меньше 1 % в крови; в костном мозге <5% | Прогноз также хороший. Если присутствует мутация в гене SF3B1, то количество кольцевых сидеробластов может превышать 5%. |
| МДС с мультилинейной дисплазией (MDS-MLD) | Снижение количества двух или более типов клеток крови *; выраженная дисплазия двух и более ростков кроветворения. | Нет или меньше 1 % в крови; в костном мозге <5% | Приблизительно в 10% случаев развивается острый лейкоз. Около половины пациентов умирают в течение 2 лет после постановки диагноза. |
| МДС с избытком бластов – 1 (MDS-EB-1) | Снижение количества одного или нескольких типов клеток крови* со значительными отклонениями или без в костном мозге. | увеличение количества бластов, но менее 10% в костном мозге (5-9%); нет палочек Ауэра | Около 25% пациентов с этим типом заболевают острым миелоидным лейкозом (ОМЛ), и большинство из них после постановки диагноза умирает в течение 2 лет. |
| МДС с избытком бластов – 2 (MDS-EB-2) | То же, что и MDS-EB-1 | Много бластов в костном мозге (10-19%) и / или крови (5-19%), или число бластов как и при MDS-EB-1, но присутствуют палочки Ауэра | У каждого второго с этим типом развивается ОМЛ; в остальных случаях причина смерти — недостаточность костного мозга. |
| МДС неклассифицированный (MDS-U) | Снижение количества одного или нескольких типов клеток крови* с выраженной дисплазия костного мозга или без неё. | Нет или редко встречаемые бласты (<1%) в крови; отсутствует увеличение бластов в костном мозге (<5%) | Тип встречается крайне редко. |
| МДС с изолированной del(5q) | Низкие эритроциты *, нормальные лейкоциты, тромбоциты могут быть снижены | Нет или редкие бласты (<1%) в крови; нет увеличения бластов в костном мозге (<5%); нет палочек Ауэра | В пораженных клетках отсутствует длинное плечо хромосомы 5 [del (5q)]. Прогноз обычно хороший. Существует 10 процентный риск перехода в острый лейкоз. Хорошо реагирует на лечение Ревлимидом (леналидомид). |
* Пороговыми значениями для МДС являются гемоглобин <10 г>
Клиническая классификация
Клиническая классификация учитывает предполагаемую причину возникновения миелодиспластического синдрома:
- Первичный (de novo) МДС — причина заболевания не определена; большинство диагностируемых миелодиспластических синдромов являются первичными.
- Вторичный МДС — причина подтверждена; это может быть предшествующая интенсивная химиотерапия или воздействие лучевой терапии. Вторичный МДС плохо поддается лечению.
Высокий риск развития заболевание связан с:
- химиотерапевтическим лечением по поводу различных раков;
- высокодозной лучевой терапией;
- воздействием:
- гербицидов, пестицидов и других удобрений;
- бензола, толуола;
- тяжелых металлов;
- химикатов, связанных с нефтяной промышленностью.
Миелодиспластический синдром (МДС) вызывает множество вопросов и обсуждений среди пациентов и врачей. Люди часто делятся своими переживаниями о диагностике, которая включает в себя анализы крови, костномозговую пункцию и цитогенетические исследования. Эти тесты помогают определить тип МДС и оценить степень заболевания. Прогностические критерии, такие как индекс IPSS, играют важную роль в оценке риска прогрессирования болезни и выбора лечения. Многие пациенты рассказывают о различных подходах к терапии, включая поддерживающее лечение, химиотерапию и трансплантацию костного мозга. Несмотря на сложности, многие находят поддержку в сообществах, где делятся опытом и советами, что помогает справляться с диагнозом и улучшать качество жизни.

Прогностическая система
В 1997 году была разработана Международная шкала оценки прогноза (IPSS), которая предусматривает присвоение низкой, средней или высокой степени риска миелодиспластическому синдрому. IPSS пересмотрена в 2012 году (IPSS-R), были включены такие факторы, описывающие болезнь: количество бластов, цитогенетика, гемоглобин, абсолютное количество нейтрофилов, количество тромбоцитов и возраст пациента. IPSS-R более точена при разработке прогноза, чем IPSS. Она помогает определить предполагаемое среднее время выживания и вероятность развития острого миелоидного лейкоза (ОМЛ).
Также разработана система прогностической оценки (WPSS) Всемирной организации здравоохранения (ВОЗ). С помощью ее строят прогноз учитывая классификацию ВОЗ, хромосомные аномалии и необходимость переливания крови.
Пациенты с низким риском живут дольше (медиана выживаемости 136 месяцев), у них реже заболевание переходит в острый миелоидный лейкоз. Важно отметить, что эти инструменты учитывают вероятность и не могут определить, что именно произойдет с конкретным человеком.
Симптомы миелодиспластического синдрома
Клинические проявления заболевания обусловлены уменьшением содержания зрелых клеток крови. В зависимости от типа клеток и степени их снижения в кровотоке, симптомы миелодиспластического синдрома группируются следующим образом:
- уменьшение количества эритроцитов (анемия):
- слабость, сонливость,
- дискомфорт или трудности при дыхании,
- повышенная усталость,
- бледность кожных покровов;
- уменьшение количества лейкоцитов (лейкопения):
- рецидивирующие инфекции,
- лихорадка;
- уменьшение количества тромбоцитов (тромбоцитопения):
- носовые кровотечения,
- склонностью к образованию синяков,
- петехии (сыпь на теле в виде крошечных красных точек на коже).

Лабораторные анализы
Цели лабораторных исследований — подтвердить диагноз, исключив другие состояния, которые могут вызывать сходные симптомы, классифицировать МДС, оценить прогноз, отследить течение заболевания и определиться с лечением.
Основной набор анализов
- Клинический (общий) анализ крови – это наиболее часто назначаемое исследование качественного и количественного состава крови, который помогают диагностировать и контролировать течение МДС, в ходе которого дается характеристика эритроцитов (их размера, формы и зрелости), лейкоцитов и их разновидностей в процентном соотношении (лейкоцитарная формула) и тромбоцитов).
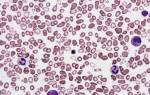
- Мазок периферической крови – этот анализ позволяет морфологически оценить клетки, присутствующие в крови. Капля крови тонко размазывается на предметном стекле, затем обрабатывается специальным красителем и исследуется под микроскопом. Анализ помогает выявить и оценить незрелые бластные клетки и клетки-предшественники или аномально выглядящие (диспластические) клетки.
- Аспирационная или трепан-биопсия костного мозга — эта процедура используется во время диагностики МДС и иногда повторяется в процессе лечения. У человека производится забор небольшого количества костного мозга и исследуются под микроскопом специалистом, который оценивает количество, размер и внешний вид различных клеток-предшественников.
- Хромосомный анализ (кариотипирование) и / или флуоресцентная гибридизация in situ (FISH) – эти анализы выполняются для выявления хромосомных аномалий, а также с целью диагностики и классификации МДС, выбора варианта лечения и оценки прогноза.
Дополнительные тесты
- Проточная цитометрия — хотя этот анализ не считается обязательным при миелодиспластическом синдроме, его, иногда, используют при диагностике и классификации заболевания, особенно в тех, случаях, когда вышеперечисленные исследования не позволяют сделать определенное заключение.
- Иммуноцитохимия — это метод морфологической диагностики, в основе которого лежит визуализация и оценка реакции антиген-антитело в клетках, которые можно увидеть под микроскопом. Анализ редко применяется при диагностике МДС, он бывает полезен при проведении дифдиагностики различных типов миелодиспластического синдрома с другими заболевание костного мозга.
- Анализы на выявление мутации в генах — если существуют показания, то проводиться тест, позволяющий определить специфические генные мутации, которые могут помочь в определении типа миелодиспластического синдрома, предсказать ответ на лечение и его результаты.
Другие лабораторные исследования
- Витамин В12 и фолат — определение других причин анемии.
- Анализы крови на железо (сывороточное железо, ферритин, общая железосвязывающая способность сыворотки и трансферрин) — исключить дефицит железа как причину анемии или диагностировать избыток.
- Эритропоэтин — помогает оценить анемию и определить сам необходимости переливания крови или лечения рекомбинантным эритропоэтином.
Лечение миелодиспластического синдрома
Лечение МДС зависит от нескольких факторов: стадии заболевания, возраста и общего состояния здоровья пациента, а также от прогноза и предполагаемого ответа на терапию. В настоящее время трансплантация стволовых клеток костного мозга считается единственным доступным способом полностью избавиться от заболевания. Данный метод лечения часто рекомендуются детям и все чаще используется и у взрослых. В случае отсутствия показаний для трансплантации стволовых клеток проводимые лечебные мероприятия при МДС направлены на облегчение симптоматики заболевания и предотвращение осложнений или прогрессирования заболевания в острый миелоидный лейкоз.
Не всем пациентам необходимо лечение. Если отсутствует анемия, нет геморрагического синдрома и инфекционных осложнений, то пациенты могут только наблюдаться (тактика «watch and wait»).
Переливание крови пациентам с МДС – одна из главных составляющих программы лечения
При наличии анемии может потребоваться переливание крови. Частые гемотрансфузии приводят к накоплению избытка железа в организме. Так как железо токсически воздействует на различные органы и ткани, возникает необходимость в постоянном приеме препараты, связывающие железо — хелаторы (десферал, эксиджад). Пациенты с низким уровнем эритропоэтина в крови (например, <500 МЕ>
Переливание тромбоцитарной массы используется при угрозе возникновения серьезного кровотечения. А также могут быть назначены лекарства, которые стимулируют выработку тромбоцитов в костном мозге (например, элтромбопаг).
Антибиотики применяются в случае лейкопении (снижение количества лейкоцитов), а также при наличии рецидивирующей инфекции. Факторы роста, такие как гранулоцитарный колониестимулирующий фактор (G-CSF) и гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), могут быть использованы для стимуляции продукции лейкоцитов.
При МДС используются химиотерапевтические средства (5-азацитидин и децитабин), иммуномодулирующие препараты, такие как леналидомид (особенно он эффективен у пациентов с изменениями хромосомы del (5q)), а также иммунодепрессанты.
Обязательно следует обсуждать со своим врачом риски и преимущества предложенного варианта лечения, узнать, почему именно данная терапия лучше всего подходит для вас.
Заметили ошибку? Выделите ее и нажмите Ctrl+Enter, чтобы сообщить нам.
Вопрос-ответ
Какие анализы необходимы для диагностики миелодиспластического синдрома?
Для диагностики миелодиспластического синдрома обычно назначаются общий анализ крови, биохимический анализ крови, а также морфологическое исследование костного мозга. Эти исследования помогают определить уровень различных клеток крови и выявить аномалии в их структуре.
Каковы основные прогностические критерии для оценки миелодиспластического синдрома?
Основные прогностические критерии включают количество бластных клеток в костном мозге, наличие хромосомных аномалий, уровень гемоглобина и тромбоцитов, а также возраст пациента. Эти факторы помогают врачам определить прогноз заболевания и выбрать наиболее подходящее лечение.
Какие методы лечения применяются при миелодиспластическом синдроме?
Лечение миелодиспластического синдрома может включать поддерживающую терапию, такую как переливание крови и препараты, стимулирующие образование клеток крови. В более тяжелых случаях может потребоваться химиотерапия или пересадка костного мозга. Выбор метода лечения зависит от конкретного типа МДС и состояния пациента.
Советы
СОВЕТ №1
Перед началом лечения обсудите с врачом все возможные варианты терапии, включая их преимущества и недостатки. Это поможет вам лучше понять, какой подход будет наиболее эффективным для вашего конкретного случая.
СОВЕТ №2
Регулярно проходите необходимые анализы и обследования, чтобы отслеживать динамику заболевания. Это позволит своевременно корректировать лечение и принимать меры при ухудшении состояния.
СОВЕТ №3
Не стесняйтесь задавать вопросы своему врачу. Понимание диагноза, прогностических критериев и возможных побочных эффектов лечения поможет вам чувствовать себя более уверенно и контролировать ситуацию.
СОВЕТ №4
Обратите внимание на свое питание и образ жизни. Здоровая диета и умеренные физические нагрузки могут поддержать ваше общее состояние и улучшить качество жизни во время лечения.